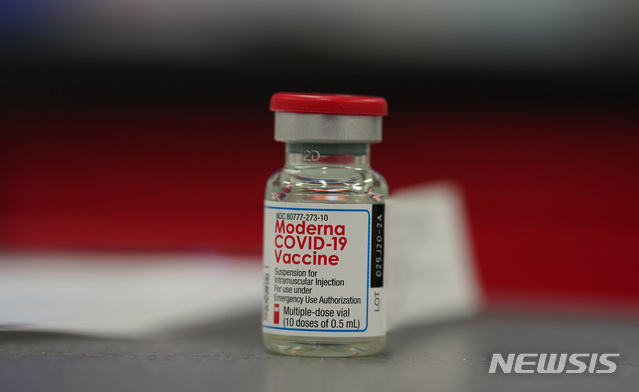
EU, 오미크론 맞춤형 화이자·모더나백신 사용 승인 화이자와 모더나가 오미크론 변이 맞춤형으로 개발한 신종 코로나바이러스 감염증(코로나19) 백신의 유럽연합(EU) 내 사용이 승인됐다. 스텔라 키리아키데스 보건 담당 유럽연합(EU) 집행위원은 2일(현지시간) 트위터에 올린 글에서 "EU 집행위는 화이자와 모더나의 오미크론 변이 맞춤형 코로나19 백신의 사용을 승인했다"고 밝혔다. 앞서 유럽의약품청(EMA)은 전날 코로나19와 오미크론을 예방하는 이들 2가 백신(개량백신)의 판매 승인을 권고했다. EMA가 오미크론 등 코로나19 하위변이를 겨냥한 맞춤형 백신을 승인 권고한 것은 이번이 처음이다. 새 백신은 기존 백신을 최소한 1차례 이상 접종받은 12세 이상에 대해 기존 접종을 받은 지 3개월이 지난 후 ..